La luz: onda o chorro de bolitas
Apuntas una luz roja al metal. Nada. Más brillante. Nada. Cambias al azul. Apenas un destello tenue. Y los electrones saltan. La onda más fuerte no puede hacer lo que la más débil logra. La explicación destruyó todo lo que creían saber sobre la luz. Capítulo 4.

A finales del siglo XIX, la naturaleza de la luz era un caso cerrado. Era una onda. Punto.

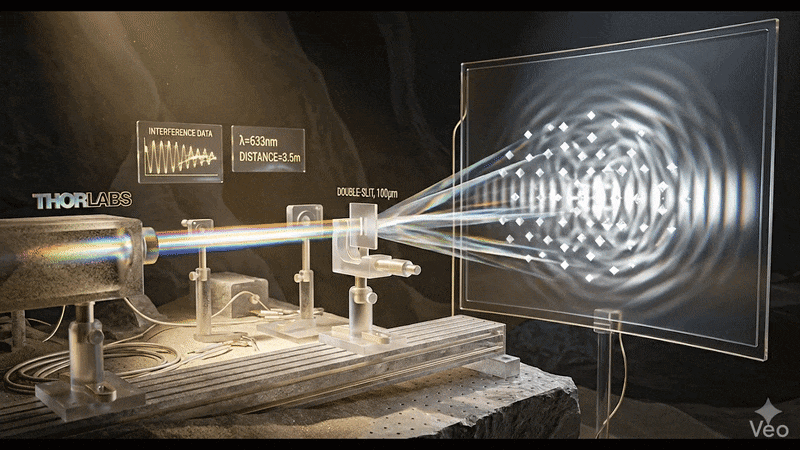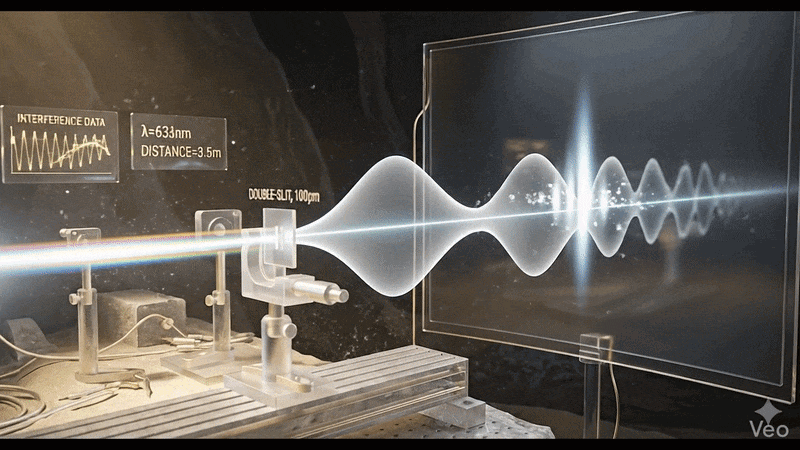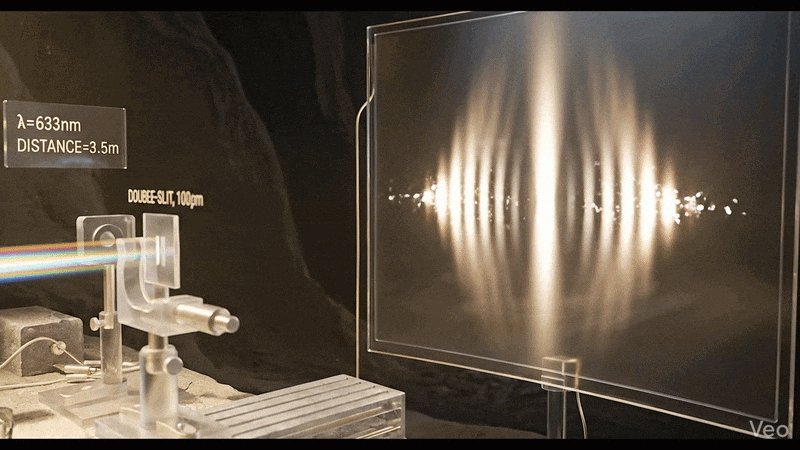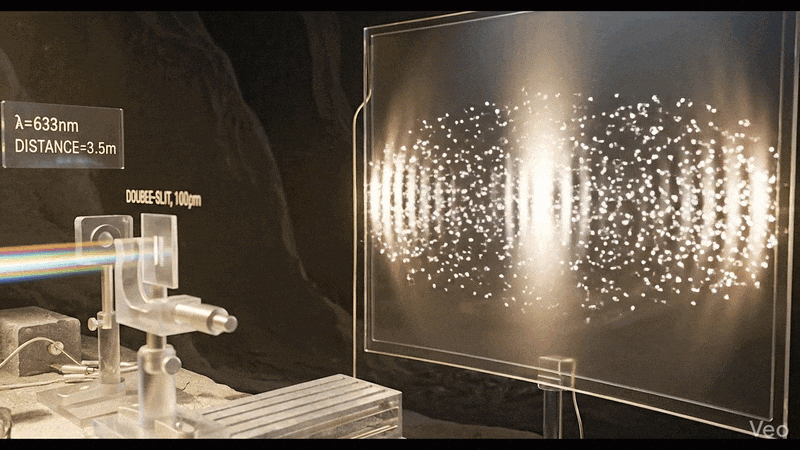
Thomas Young lo había demostrado un siglo antes: hizo pasar luz por dos rendijas y observó interferencia. Solo las ondas hacen eso.
Entonces alguien iluminó una placa de metal. Y la luz hizo algo que ninguna onda debería poder hacer.
El experimento que no tenía sentido
Si iluminas una placa de metal con luz, a veces el metal emite electrones. La luz los "arranca" del material. Esto se llamó efecto fotoeléctrico.
Parecía simple. La luz lleva energía.
La energía arranca electrones.
¿Qué tiene de misterioso?
El misterio apareció cuando midieron los detalles.
Tres pistas que no encajaban
Si la luz es una onda, su energía depende de su intensidad (qué tan brillante es). Una luz más brillante debería darle más energía a los electrones arrancados.
Pero eso no es lo que observaron.
Pista 1: La energía de los electrones no depende del brillo.
Puedes hacer la luz diez veces más brillante. Los electrones salen con la misma energía. Solo salen más electrones, no electrones más rápidos.
Extraño.
Pista 2: La energía de los electrones depende del color.
Luz azul produce electrones más energéticos que luz roja, sin importar el brillo. El color importa. La intensidad no.
Más extraño aún.
Pista 3: Hay un color mínimo. Debajo de él, no pasa nada.
Si usas luz roja muy intensa, no arrancas ningún electrón. Cero. Puedes esperar horas. Nada.
Pero con luz azul tenue (mucho menos brillante) los electrones salen de inmediato.
¿Cómo puede una onda débil hacer algo que una onda fuerte no puede?

El problema con las ondas
Si la luz fuera una onda continua, esto no tendría sentido.
Imagina olas golpeando una roca en la playa. Si las olas son suaves pero continuas, eventualmente acumulan suficiente energía para mover la roca. Solo necesitas esperar.
Olas más grandes la moverían más rápido. Olas más pequeñas tardarían más. Pero eventualmente, cualquier ola debería poder hacerlo.
Con la luz y los electrones, no funciona así.
La luz roja, sin importar cuánto tiempo esperes ni cuán intensa sea, nunca arranca electrones de ciertos metales. Nunca. Es como si las olas rojas simplemente no pudieran mover esa roca, sin importar cuántas lleguen.
Pero las olas azules, aunque sean pequeñas, la mueven al instante.
¿Qué está pasando?

La idea audaz de Einstein
En 1905, Albert Einstein (entonces un empleado desconocido de una oficina de patentes en Suiza) propuso una solución radical.
La luz no es una onda continua. Viene en paquetes discretos de energía.
Cada paquete tiene una cantidad fija de energía que depende del color (la frecuencia) de la luz:
$$E = h \times f$$
Donde $f$ es la frecuencia de la luz y $h$ es la constante de Planck, un número increíblemente pequeño que aparece en toda la física cuántica.
Luz azul tiene alta frecuencia. Paquetes con mucha energía.
Luz roja tiene baja frecuencia. Paquetes con poca energía.
Einstein llamó a estos paquetes cuantos de luz. Hoy los llamamos fotones.
Cada fotón individual es diminuto. Una bombilla común emite billones de ellos por segundo. Por eso no notamos los paquetes: es como ver una playa y no distinguir los granos de arena. Pero a escala atómica, la granularidad importa. Los átomos absorben un fotón a la vez.
Cómo esto explica todo
Con la idea de los fotones, las tres pistas encajan perfectamente.
¿Por qué la energía de los electrones depende del color?
Cada electrón absorbe un fotón. Un fotón azul tiene más energía que uno rojo. El electrón sale con más velocidad.
¿Por qué el brillo no aumenta la energía?
Más brillo significa más fotones, no fotones más energéticos. Cada electrón sigue absorbiendo un solo fotón. Más fotones significan más electrones arrancados, pero cada uno con la misma energía.
¿Por qué hay un color mínimo?
Para arrancar un electrón del metal, necesitas una energía mínima. Si el fotón no tiene suficiente energía, no puede arrancar nada. No importa cuántos fotones envíes: si cada uno es demasiado débil, ninguno hace el trabajo.
Es como tratar de romper una ventana con pelotas de ping-pong. Puedes lanzar millones. Ninguna tiene suficiente energía por sí sola para romper el vidrio. Pero una sola piedra (aunque sea más pequeña) lo logra porque concentra su energía en un solo impacto.

Newton tenía razón (más o menos)
¿Te das cuenta de lo que acaba de pasar?
Newton decía que la luz eran partículas. Young demostró que era una onda. Caso cerrado.
Y ahora Einstein demuestra que también son partículas.
No es que Young estuviera equivocado. La luz sí interfiere. Sí se comporta como onda. Pero cuando golpea un átomo, llega como un paquete indivisible. Una partícula.
Onda y partícula. No una u otra. Las dos.
Si esto te recuerda a la doble rendija, debería. Los electrones hacen exactamente lo mismo. El universo, a escala cuántica, se niega a elegir entre nuestras categorías.
El hombre que encendió el fuego
Por este trabajo (no por la relatividad) Einstein ganó el Premio Nobel de Física en 1921. La mayoría de la gente se sorprende al escuchar esto. Pero el comité tenía razón: los fotones no solo explicaron un experimento. Rompieron nuestra concepción de la luz.
Y aquí viene la ironía más deliciosa de la física moderna.
Einstein encendió la chispa de la mecánica cuántica. Pero pasó el resto de su vida tratando de apagar el incendio.
La mecánica cuántica (la teoría que él ayudó a crear) implica probabilidad fundamental, superposiciones, colapso. Y Einstein nunca lo aceptó.
"Dios no juega a los dados", dijo.
La respuesta de Bohr fue implacable: "Deja de decirle a Dios lo que tiene que hacer."
Esa pelea (la más grande de la historia de la física) la contaremos en su momento.

Resumen: lo que acabamos de aprender
- El efecto fotoeléctrico mostró comportamiento inexplicable si la luz es una onda pura.
- La energía de los electrones depende del color (frecuencia), no del brillo.
- Einstein propuso que la luz viene en paquetes discretos llamados fotones: $E = h \times f$.
- La luz es onda y partícula a la vez, igual que los electrones.
- Einstein ganó el Nobel por esto, e irónicamente nunca aceptó las consecuencias de lo que inició.
Lo que viene
Einstein usó los cuantos para explicar la luz. Pero no inventó la idea. La tomó prestada.
Cinco años antes, Max Planck había inventado los cuantos por desesperación. La física clásica predecía que cualquier objeto caliente debería emitir energía infinita. Tu estufa debería destruir el universo cada vez que la enciendes.
Obviamente, no lo hace. Pero explicar por qué no lo hace requirió romper la física.
"Fue como si el suelo hubiera cedido bajo mis pies, sin que apareciera ninguna base firme sobre la cual construir." — Albert Einstein, sobre la revolución cuántica
Siguiente: Capítulo 5 — "El color de las cosas calientes (y por qué casi destruye la física)"